Место Ритмокора в комплексной антиаритмической терапии у пациентов с патологией щитовидной железы
Публикация обновлена: Июль 19
По данным ВОЗ патологией щитовидной железы страдает более 200 млн. человек в мире. Только за последние 5 лет абсолютный прирост числа вновь выявленных заболеваний в экономически развитых странах составил 51,8% среди женщин и 16,7% среди мужчин. По данным Фремингемского исследования, повышенный уровень ТТГ отмечен у 13,6% женщин, а в Колорадском исследовании – у 9,5% лиц [1].
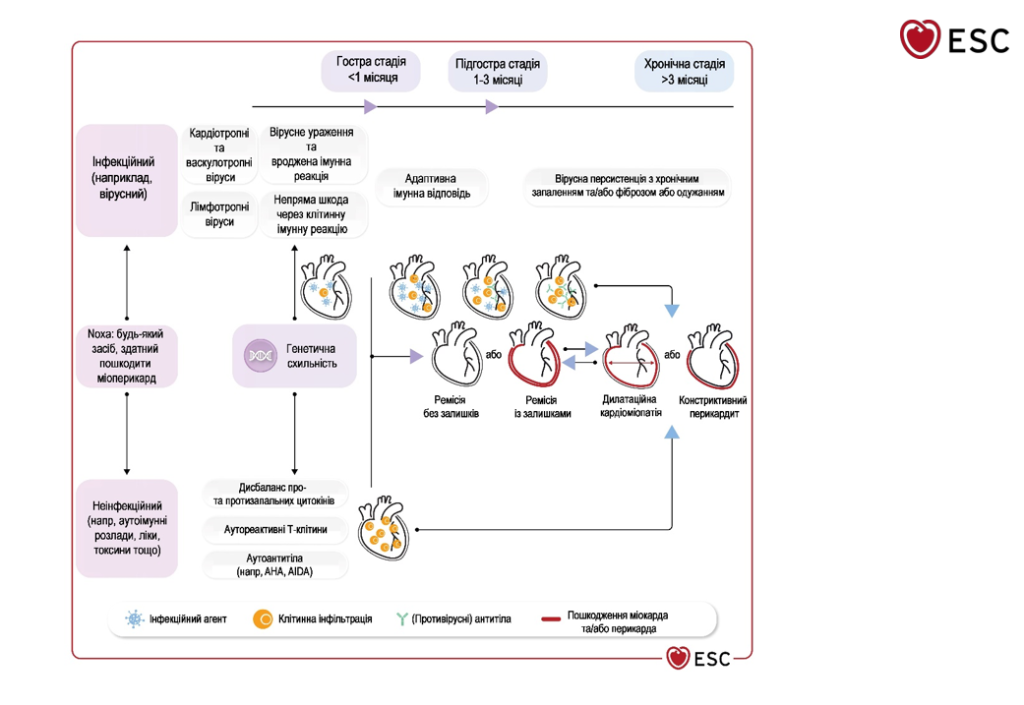
Давно известно, что основные клинические проявления и симптомы заболеваний ЩЖ связаны с эффектом воздействия тиреоидных гормонов на сердечно-сосудистую систему. Как избыток, так и недостаток тиреоидных гормонов вызывает изменения сердечной сократимости, сердечного выброса, артериального давления и общего периферического сосудистого сопротивления (ОПСС) [2, 3]. В большинстве случаев сердечно-сосудистые изменения обратимы при нормализации функции ЩЖ. В последние десятилетия показано, что и субклинические нарушения функции ЩЖ могут оказывать эффект на сердечно-сосудистую систему и увеличивать сердечно-сосудистый риск. Становится все более очевидным, что и острая, и хроническая сердечно-сосудистая патология может изменять обмен тиреоидных гормонов и тем самым вносить свой вклад в прогрессирование сердечно-сосудистой недостаточности [4].
Патология сердца при дисфункции щитовидной железы зачастую является ведущей в клинике заболевания и нередко приводит к утрате трудоспособности, а при тяжелом течении и к смерти у этой категории больных. В клинической картине отмечаются разнообразные сложные нарушения ритма сердца, артериальная гипертензия, метаболическая кардиомиопатия с развитием хронической сердечной недостаточности. Морфофункциональным изменениям миокарда всегда предшествуют метаболические нарушения в сердечной мышце. Изменения сердечно-сосудистой системы при гипертиреозе обусловлены воздействием избыточного количества тиреоидных гормонов на обменные процессы и гемодинамику. Одним из важных эффектов тиреоидных гормонов является разобщение окислительного фосфорилирования, что приводит к снижению в сердечной мышце содержания АТФ и креатинфосфата. В результате происходит угнетение анаболических процессов: снижается синтез и усиливается распад гликогена и белка, снижается содержание калия в миоцитах и других клетках. Потребление кислорода миокардом увеличивается, однако эффективность его утилизации в процессе биологического окисления снижается. При избытке тироксина нарушается проницаемость митохондриальных мембран [4, 7]. Под влиянием тиреоидных гормонов происходит усиление сократительной функции миокарда, вероятно, вследствие активизации стимулирующего влияния на сердце и прямого действия тироксина на сердечную мышцу.
Избыток тиреоидных гормонов изменяет симпатические и парасимпатические влияния на миокард. При высокой степени тиреотоксикоза при длительном его течении в результате резкого снижения эффективности биологического окисления, преобладания распада белка над его синтезом снижается уровень энергетических ресурсов и пластических процессов, что приводит к угнетению сократительной функции миокарда [1, 4, 7]. Снижение уровня тиреоидных гормонов в организме, даже ничтожный дефицит, также обусловливает серьезные нарушения обменных процессов, в том числе дистрофические изменения в сердце, сопровождающиеся снижением интенсивности окислительного фосфорилирования, замедлением синтеза белка, уменьшением поглощения кислорода миокардом, электролитными сдвигами. Поражается как сократительный миокард, так и строма. В кардиомиоцитах откладывается креатинфосфат и возникает, так называемая, псевдогипертрофия миокарда. В сердце, как и в других тканях, депонируются кислые гликозаминогликаны, приводящие к слизистому отеку миокарда и стромы [1, 7]. Важно раннее выявление патологии сердца до манифестации клинических симптомов, что возможно при скрининговом обследовании.
Основой для развития аритмии сердца у пациентов с патологией щитовидной железы являются различные патофизиологические сдвиги, развивающиеся под влиянием действия гормонов щитовидной железы, которая секретирует 2 вида гормонов (Т3 и Т4). Физиологическое действие гормонов связывают в большей степени с трийодтиронином (Т3), который активнее тироксина (Т4) в 4-5 раз. В сутки секретируется около 100 мкмоль тироксина и 5 мкмоль трийодтиронина. 99,96% указанных гормонов находятся в связанной с белками форме и депонируются. Биологическая активность тиреотропных гормонов (ТГ) осуществляется за счет остальных 0,4% указанных гормонов.
Основные эффекты ТГ реализуются на уровне клеточного ядра, изменяя экспрессию генома, а также вне генома через воздействие на плазматическую мембрану клетки (регулируя поток субстратов и катионов в клетку и из нее), цитоплазму, митохондрии (влияя на окислительный обмен). В механизмах негеномных эффектов могут участвовать компоненты систем передачи сигналов вклетку: фосфолипид или Са-зависимая протеинкиназа, цАМФ-зависимая протеинкиназа, комплекс кальмодулин — Са. К негеномным эффектам ТГ относятся: регуляция внутриклеточного уровня некоторых ионов и их распределение внутри клетки.
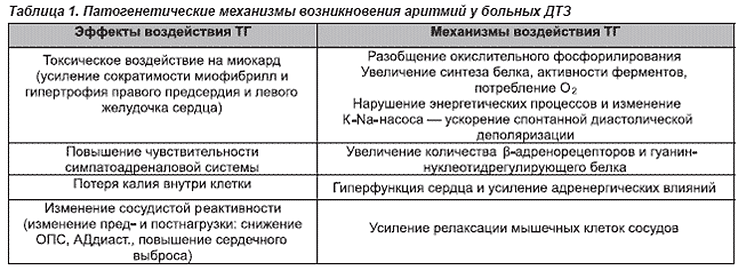
Патогенез аритмий при избытке тиреоидных гормонов до конца не изучен, и в настоящее время в их развитии придают значение таким факторам: токсическое воздействие ТГ на миокард, повышение симпатического тонуса вегетативной нервной системы, снижение внутриклеточного калия (табл. 1). Истощение нормотопной функции синусового узла вследствие уменьшения запасов субстрата автоматизма — ацетилхолина также ведет к развитию синдрома слабости синусового узла и переходу на патологический ритм.
Кардиопротекторы – это фармакологические средства профилактики нарушений и оптимизации функции сердца при нормальных физиологических и патологических условиях. Данный термин, выделяющий целый класс препаратов цитопротекторного и метаболического действия, применяемых для коррекции и восстановления функционального состояния миокарда, появился в медицинской и научной терминологии еще в 1990-х годах [69]. На сегодня сформировалась точка зрения, согласно которой кардиопротекторы – это лекарственные препараты разных химических классов, действие которых не связано с гемодинамическим эффектом, а опосредуется оптимизацией процессов образования и расхода энергии, коррекцией функции дыхательной цепи, нормализацией баланса между интенсивностью процессов свободнорадикального окисления и антиоксидантной защитой, непосредственным влиянием на кардиомиоциты, что способствует их выживаемости в условиях ишемии, препятствует формированию метаболического ремоделирования (изменения) миокарда. [7].
Механизм действия кардиопротекторов разнообразный и многоплановый, поэтому необходимо разделить фармакологические средства данной категории на виды по их биологическим свойствам и иным факторам [69] (рис. 1). Так, существует разделение кардиопротекторов на два больших типа: прямого и непрямого действия. Активность первых обусловливается как местным (стабилизация мембран, сосудорасширяющий эффект, влияние на процесс обмена веществ в кардиомиоцитах), так и центральным воздействием (регуляция сосудистого тонуса благодаря влиянию на структурные элементы ЦНС). Вторые же примечательны тем, что способны уменьшать нагрузку на миокард и вследствие этого предупреждать метаболические нарушения в кардиомиоцитах.
Принципиальным отличием в механизме действия недавно разработанного препарата “Ритмокор” (фармацевтическая фирма "ФарКоС"), является активация обмена глюкозы при ишемии, без блокады окисления жирных кислот в нормоксических условиях. Действующим веществом препарата является пентаоксикапроновая кислота в виде магниевой и калиевой солей, обладающая метаболическим, мембраностабилизирующим, антиоксидантным и антиаритмическим действием [4]. Метаболическая активность препарата определяется активацией пентозофосфатного цикла (гексозомонофосфатный шунт) - сложного ферментативного процесса прямого аэробного окисления фосфорилированной глюкозы до CO2 и H2O, сопровождающийся накоплением важного кофермента — восстановленного никотинамидадениндинуклеотидфосфата (НАДФ×Н) (рис. 2). Установлено, что парентеральное введение ритмокора на фоне базисной терапии улучшает переносимость физических нагрузок и уменьшает клинические проявления стенокардии напряжения у больных пожилого возраста [4], а также оказывает выраженный антиаритмический эффект [7].
В ходе экспериментальных исследований установлено, что ритмокор в условиях ишемии стимулирует пентозофосфатный путь окисления глюкозы, способствует угнетению процессов перекисного окисления липидов и свободнорадикального окисления белков, нормализует активность основных ферментов метаболизма миокарда лактатдегидрогеназы, креатинфосфокиназы, сукцинатдегидрогеназы, а также способствует нормализации ионного гомеостаза [7].
Известно, что магний в состоянии способствовать нормализации внутриклеточного содержания ионов натрия, калия и кальция, что тем самым ведет к улучшению коронарного кровообращения вследствие снижения тонуса сосудов и уменьшения миокардального потребления кислорода, предотвращению некроза клеток и их электрической стабилизации [9,12].
Кроме того, существует целый ряд клинических ситуаций, при которых ритмокору может быть отдано предпочтение в сравнении с другими метаболическими препаратами-наличие нарушений сердечного ритма, изменение уровня калия, магния, натрия в сыворотке крови, при непереносимости антиангинальных средств основных классов и при ограничениях или противопоказаниях к их назначению.
Благоприятное влияние на метаболизм обусловлено повышением активности окислительно-восстановительных ферментов, в частности Na+/K+-АТФ-азы [10], что, в cвою очередь, способствует повышению стабильности электрофизиологических свойств кардиомиоцитов.
При экспериментальном моделировании нарушений сердечного ритма антиаритмический эффект Ритмокора сопоставим с эффектами амиодарона [9-11]. Ритмокор обладает широким спектром антиаритмической активности в т.ч. снижает риск развития желудочковой тахикардии и экстрасистолии высоких градаций.
Глюконовая кислота и ее соли обладают свойством нормализовать нарушенный баланс калия и натрия в миокарде при коронарной недостаточности (повышается содержание калия и снижается содержание натрия), что обусловливает антиаритмическое действие в условиях экспериментального моделирования ишемии сердца [8].
По результатам экспериментальных исследований, Ритмокор улучшает клеточный метаболизм, оказывает мембраностабилизирующее, антиаритмическое и антиоксидантное действие [9].
Опыт клинического применения препарата до последнего времени ограничивался исследованием антиаритмической эффективности и переносимости капсулированной формы препарата.
Целью данного исследования является комплексный анализ антиаритмической активности, оценка эффективности и безопасности курсового приема Ритмокора у пациентов с диффузным токсическим зобом в состоянии компенсации в дополнение к базовой терапии бета-блокаторами, которая используется в Украине согласно стандартам ведения таких пациентов по схеме: Ритмокор по 15 мл 10 % раствора внутривенно 10 дней, далее по 1 капсулы 3 раза в день в течении 1 месяца.
Данное клиническое исследование проводилось как наблюдательное (неинтервенционное), открытое, контролируемое, несравнительное, проспективное исследование, в котором ЛС «Ритмокор» назначался в соответствии с зарегистрированными показаниями. В исследовании не проводились дополнительные мониторинговые процедуры, а обследование пациентов выполнялось в рамках обычной рутинной медицинской практики. В исследовании приняли участие 25 пациентов (средний возраст = 43±6 лет , 5 мужчин, 20 женщин), которые получали лечение в Государственном учреждении «Институт эндокринологии и обмена веществ им. В.П.Комиссаренко НАМН Украины» по поводу диффузного токсического зоба.
В исследование не включали пациентов со всеми формами фибрилляции предсердий, с некорригируемым артериальным давлением (АД) > 160/90 мм рт. ст., снижением ФВ < 40 % по данным двухмерной эхокардиографии (ЭхоКГ), перенесших инфаркт миокарда и инсульт, клинически выраженной сердечной недостаточностью, значительно выраженными нарушениями функции почек и печени, с наркотической или алкогольной зависимостью, перенесенными острыми воспалительными заболеваниями в течение предшествующего месяца. Также в исследовании не принимали участие пациенты, перенесшие реваскуляризацию, с нестабильной стенокардией или инфарктом миокарда и ревматическими пороками сердца.
Также все пациенты проходили общепринятое клиническое, лабораторное (общий анализ крови и мочи, определение липидного профиля, уровня креатинина, мочевины, глюкозы, аспартатаминотрансферазы, аланинаминотрансферазы, билирубина) и инструментальное исследование ( электрокардиография с оценкой ВРС, холтеровское мониторирование ЭКГ).
Исследование ВРС проводилось на диагностическом комплексе “Cardio” с использованием статистического анализа временной области и спектрального анализа короткой (пятиминутной) последовательности электрокардиографических интервалов R–R в состоянии покоя. Определялись следующие показатели временного анализа: стандартное отклонение (SDnn, мс), стандартное отклонение разностей продолжительности соседних интервалов R–R (RMSSD, мс). При выполнении спектрального анализа определялись: общая мощность спектра ритма сердца (tP, мс2), мощности в диапазоне 0,00–0,04 Гц (Vlf, мс2), 0,04–0,15 Гц (lf, мс2), 0,15–0,4 Гц (hf, мс2) и соотношение lf/hf. Спектральные составляющие lf и hf анализировались как в абсолютных значениях, так и в производных от них нормализованных единицах (н.е.), которые автоматически рассчитывались по формулам: lfnorm = lf / (tP – Vlf) × 100 % и hfnorm = hf / (tP – Vlf) × 100 %. Определялась также структура спектра в процентном соотношении составляющих: %Vlf, %lf, %hf.
Исследование предполагало три визита пациента к врачу (таб. 2).
Полный текст публикации внизу.
Давно известно, что основные клинические проявления и симптомы заболеваний ЩЖ связаны с эффектом воздействия тиреоидных гормонов на сердечно-сосудистую систему. Как избыток, так и недостаток тиреоидных гормонов вызывает изменения сердечной сократимости, сердечного выброса, артериального давления и общего периферического сосудистого сопротивления (ОПСС) [2, 3]. В большинстве случаев сердечно-сосудистые изменения обратимы при нормализации функции ЩЖ. В последние десятилетия показано, что и субклинические нарушения функции ЩЖ могут оказывать эффект на сердечно-сосудистую систему и увеличивать сердечно-сосудистый риск. Становится все более очевидным, что и острая, и хроническая сердечно-сосудистая патология может изменять обмен тиреоидных гормонов и тем самым вносить свой вклад в прогрессирование сердечно-сосудистой недостаточности [4].
Патология сердца при дисфункции щитовидной железы зачастую является ведущей в клинике заболевания и нередко приводит к утрате трудоспособности, а при тяжелом течении и к смерти у этой категории больных. В клинической картине отмечаются разнообразные сложные нарушения ритма сердца, артериальная гипертензия, метаболическая кардиомиопатия с развитием хронической сердечной недостаточности. Морфофункциональным изменениям миокарда всегда предшествуют метаболические нарушения в сердечной мышце. Изменения сердечно-сосудистой системы при гипертиреозе обусловлены воздействием избыточного количества тиреоидных гормонов на обменные процессы и гемодинамику. Одним из важных эффектов тиреоидных гормонов является разобщение окислительного фосфорилирования, что приводит к снижению в сердечной мышце содержания АТФ и креатинфосфата. В результате происходит угнетение анаболических процессов: снижается синтез и усиливается распад гликогена и белка, снижается содержание калия в миоцитах и других клетках. Потребление кислорода миокардом увеличивается, однако эффективность его утилизации в процессе биологического окисления снижается. При избытке тироксина нарушается проницаемость митохондриальных мембран [4, 7]. Под влиянием тиреоидных гормонов происходит усиление сократительной функции миокарда, вероятно, вследствие активизации стимулирующего влияния на сердце и прямого действия тироксина на сердечную мышцу.
Избыток тиреоидных гормонов изменяет симпатические и парасимпатические влияния на миокард. При высокой степени тиреотоксикоза при длительном его течении в результате резкого снижения эффективности биологического окисления, преобладания распада белка над его синтезом снижается уровень энергетических ресурсов и пластических процессов, что приводит к угнетению сократительной функции миокарда [1, 4, 7]. Снижение уровня тиреоидных гормонов в организме, даже ничтожный дефицит, также обусловливает серьезные нарушения обменных процессов, в том числе дистрофические изменения в сердце, сопровождающиеся снижением интенсивности окислительного фосфорилирования, замедлением синтеза белка, уменьшением поглощения кислорода миокардом, электролитными сдвигами. Поражается как сократительный миокард, так и строма. В кардиомиоцитах откладывается креатинфосфат и возникает, так называемая, псевдогипертрофия миокарда. В сердце, как и в других тканях, депонируются кислые гликозаминогликаны, приводящие к слизистому отеку миокарда и стромы [1, 7]. Важно раннее выявление патологии сердца до манифестации клинических симптомов, что возможно при скрининговом обследовании.
Основой для развития аритмии сердца у пациентов с патологией щитовидной железы являются различные патофизиологические сдвиги, развивающиеся под влиянием действия гормонов щитовидной железы, которая секретирует 2 вида гормонов (Т3 и Т4). Физиологическое действие гормонов связывают в большей степени с трийодтиронином (Т3), который активнее тироксина (Т4) в 4-5 раз. В сутки секретируется около 100 мкмоль тироксина и 5 мкмоль трийодтиронина. 99,96% указанных гормонов находятся в связанной с белками форме и депонируются. Биологическая активность тиреотропных гормонов (ТГ) осуществляется за счет остальных 0,4% указанных гормонов.
Основные эффекты ТГ реализуются на уровне клеточного ядра, изменяя экспрессию генома, а также вне генома через воздействие на плазматическую мембрану клетки (регулируя поток субстратов и катионов в клетку и из нее), цитоплазму, митохондрии (влияя на окислительный обмен). В механизмах негеномных эффектов могут участвовать компоненты систем передачи сигналов вклетку: фосфолипид или Са-зависимая протеинкиназа, цАМФ-зависимая протеинкиназа, комплекс кальмодулин — Са. К негеномным эффектам ТГ относятся: регуляция внутриклеточного уровня некоторых ионов и их распределение внутри клетки.
Патогенез аритмий при избытке тиреоидных гормонов до конца не изучен, и в настоящее время в их развитии придают значение таким факторам: токсическое воздействие ТГ на миокард, повышение симпатического тонуса вегетативной нервной системы, снижение внутриклеточного калия (табл. 1). Истощение нормотопной функции синусового узла вследствие уменьшения запасов субстрата автоматизма — ацетилхолина также ведет к развитию синдрома слабости синусового узла и переходу на патологический ритм.
Кардиопротекторы – это фармакологические средства профилактики нарушений и оптимизации функции сердца при нормальных физиологических и патологических условиях. Данный термин, выделяющий целый класс препаратов цитопротекторного и метаболического действия, применяемых для коррекции и восстановления функционального состояния миокарда, появился в медицинской и научной терминологии еще в 1990-х годах [69]. На сегодня сформировалась точка зрения, согласно которой кардиопротекторы – это лекарственные препараты разных химических классов, действие которых не связано с гемодинамическим эффектом, а опосредуется оптимизацией процессов образования и расхода энергии, коррекцией функции дыхательной цепи, нормализацией баланса между интенсивностью процессов свободнорадикального окисления и антиоксидантной защитой, непосредственным влиянием на кардиомиоциты, что способствует их выживаемости в условиях ишемии, препятствует формированию метаболического ремоделирования (изменения) миокарда. [7].
Механизм действия кардиопротекторов разнообразный и многоплановый, поэтому необходимо разделить фармакологические средства данной категории на виды по их биологическим свойствам и иным факторам [69] (рис. 1). Так, существует разделение кардиопротекторов на два больших типа: прямого и непрямого действия. Активность первых обусловливается как местным (стабилизация мембран, сосудорасширяющий эффект, влияние на процесс обмена веществ в кардиомиоцитах), так и центральным воздействием (регуляция сосудистого тонуса благодаря влиянию на структурные элементы ЦНС). Вторые же примечательны тем, что способны уменьшать нагрузку на миокард и вследствие этого предупреждать метаболические нарушения в кардиомиоцитах.
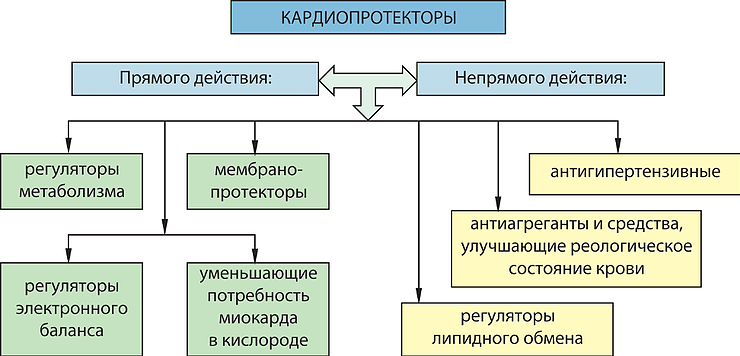
Рисунок 1. Классификация кардиопротекторов
Принципиальным отличием в механизме действия недавно разработанного препарата “Ритмокор” (фармацевтическая фирма "ФарКоС"), является активация обмена глюкозы при ишемии, без блокады окисления жирных кислот в нормоксических условиях. Действующим веществом препарата является пентаоксикапроновая кислота в виде магниевой и калиевой солей, обладающая метаболическим, мембраностабилизирующим, антиоксидантным и антиаритмическим действием [4]. Метаболическая активность препарата определяется активацией пентозофосфатного цикла (гексозомонофосфатный шунт) - сложного ферментативного процесса прямого аэробного окисления фосфорилированной глюкозы до CO2 и H2O, сопровождающийся накоплением важного кофермента — восстановленного никотинамидадениндинуклеотидфосфата (НАДФ×Н) (рис. 2). Установлено, что парентеральное введение ритмокора на фоне базисной терапии улучшает переносимость физических нагрузок и уменьшает клинические проявления стенокардии напряжения у больных пожилого возраста [4], а также оказывает выраженный антиаритмический эффект [7].
В ходе экспериментальных исследований установлено, что ритмокор в условиях ишемии стимулирует пентозофосфатный путь окисления глюкозы, способствует угнетению процессов перекисного окисления липидов и свободнорадикального окисления белков, нормализует активность основных ферментов метаболизма миокарда лактатдегидрогеназы, креатинфосфокиназы, сукцинатдегидрогеназы, а также способствует нормализации ионного гомеостаза [7].
Известно, что магний в состоянии способствовать нормализации внутриклеточного содержания ионов натрия, калия и кальция, что тем самым ведет к улучшению коронарного кровообращения вследствие снижения тонуса сосудов и уменьшения миокардального потребления кислорода, предотвращению некроза клеток и их электрической стабилизации [9,12].
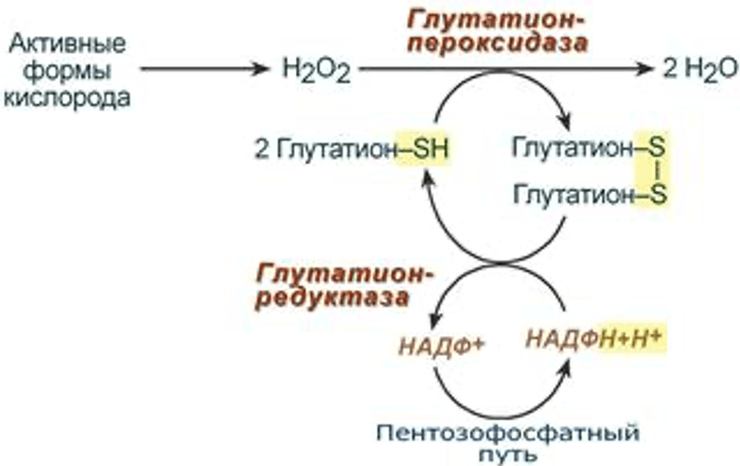
Рисунок 2. Пентозофосфатный цикл
Кроме того, существует целый ряд клинических ситуаций, при которых ритмокору может быть отдано предпочтение в сравнении с другими метаболическими препаратами-наличие нарушений сердечного ритма, изменение уровня калия, магния, натрия в сыворотке крови, при непереносимости антиангинальных средств основных классов и при ограничениях или противопоказаниях к их назначению.
Благоприятное влияние на метаболизм обусловлено повышением активности окислительно-восстановительных ферментов, в частности Na+/K+-АТФ-азы [10], что, в cвою очередь, способствует повышению стабильности электрофизиологических свойств кардиомиоцитов.
При экспериментальном моделировании нарушений сердечного ритма антиаритмический эффект Ритмокора сопоставим с эффектами амиодарона [9-11]. Ритмокор обладает широким спектром антиаритмической активности в т.ч. снижает риск развития желудочковой тахикардии и экстрасистолии высоких градаций.
Глюконовая кислота и ее соли обладают свойством нормализовать нарушенный баланс калия и натрия в миокарде при коронарной недостаточности (повышается содержание калия и снижается содержание натрия), что обусловливает антиаритмическое действие в условиях экспериментального моделирования ишемии сердца [8].
По результатам экспериментальных исследований, Ритмокор улучшает клеточный метаболизм, оказывает мембраностабилизирующее, антиаритмическое и антиоксидантное действие [9].
Опыт клинического применения препарата до последнего времени ограничивался исследованием антиаритмической эффективности и переносимости капсулированной формы препарата.
Целью данного исследования является комплексный анализ антиаритмической активности, оценка эффективности и безопасности курсового приема Ритмокора у пациентов с диффузным токсическим зобом в состоянии компенсации в дополнение к базовой терапии бета-блокаторами, которая используется в Украине согласно стандартам ведения таких пациентов по схеме: Ритмокор по 15 мл 10 % раствора внутривенно 10 дней, далее по 1 капсулы 3 раза в день в течении 1 месяца.
Данное клиническое исследование проводилось как наблюдательное (неинтервенционное), открытое, контролируемое, несравнительное, проспективное исследование, в котором ЛС «Ритмокор» назначался в соответствии с зарегистрированными показаниями. В исследовании не проводились дополнительные мониторинговые процедуры, а обследование пациентов выполнялось в рамках обычной рутинной медицинской практики. В исследовании приняли участие 25 пациентов (средний возраст = 43±6 лет , 5 мужчин, 20 женщин), которые получали лечение в Государственном учреждении «Институт эндокринологии и обмена веществ им. В.П.Комиссаренко НАМН Украины» по поводу диффузного токсического зоба.
В исследование не включали пациентов со всеми формами фибрилляции предсердий, с некорригируемым артериальным давлением (АД) > 160/90 мм рт. ст., снижением ФВ < 40 % по данным двухмерной эхокардиографии (ЭхоКГ), перенесших инфаркт миокарда и инсульт, клинически выраженной сердечной недостаточностью, значительно выраженными нарушениями функции почек и печени, с наркотической или алкогольной зависимостью, перенесенными острыми воспалительными заболеваниями в течение предшествующего месяца. Также в исследовании не принимали участие пациенты, перенесшие реваскуляризацию, с нестабильной стенокардией или инфарктом миокарда и ревматическими пороками сердца.
Также все пациенты проходили общепринятое клиническое, лабораторное (общий анализ крови и мочи, определение липидного профиля, уровня креатинина, мочевины, глюкозы, аспартатаминотрансферазы, аланинаминотрансферазы, билирубина) и инструментальное исследование ( электрокардиография с оценкой ВРС, холтеровское мониторирование ЭКГ).
Исследование ВРС проводилось на диагностическом комплексе “Cardio” с использованием статистического анализа временной области и спектрального анализа короткой (пятиминутной) последовательности электрокардиографических интервалов R–R в состоянии покоя. Определялись следующие показатели временного анализа: стандартное отклонение (SDnn, мс), стандартное отклонение разностей продолжительности соседних интервалов R–R (RMSSD, мс). При выполнении спектрального анализа определялись: общая мощность спектра ритма сердца (tP, мс2), мощности в диапазоне 0,00–0,04 Гц (Vlf, мс2), 0,04–0,15 Гц (lf, мс2), 0,15–0,4 Гц (hf, мс2) и соотношение lf/hf. Спектральные составляющие lf и hf анализировались как в абсолютных значениях, так и в производных от них нормализованных единицах (н.е.), которые автоматически рассчитывались по формулам: lfnorm = lf / (tP – Vlf) × 100 % и hfnorm = hf / (tP – Vlf) × 100 %. Определялась также структура спектра в процентном соотношении составляющих: %Vlf, %lf, %hf.
Исследование предполагало три визита пациента к врачу (таб. 2).
Полный текст публикации внизу.