Комбінована ліпідознижувальна терапія
Публікацію оновлено: Липень 11
Серцево -судинні захворювання (ССЗ) є основною причиною смерті у всьому світі. Призначення статинів для первинної та вторинної профілактики ССЗ зменшує ризики несприятливих серцево-судинних подій завдяки зниженню холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ). Однак у деяких клінічних випадках, попри застосування високодозової терапії статинами, у пацієнтів зберігаються залишкові серцево-судинні ризики, зокрема через недостатню ефективність монотерапії. Альтернативою для такої когорти пацієнтів може бути комбінація статинів з езетимібом.
Як відомо, ССЗ становлять основну причину смерті в усьому світі [1]. Зокрема, 2019 року серед загальної кількості 56,5 млн смертей 32,8% (18,6 млн були пов’я- зані із ССЗ, що вище на 17,8% (10,1 млн) смертей від новоутворень [2]. До найпоширеніших причин смерті від ССЗ належать: ішемічна хвороба серця (2,0%; 1,2 млн) та гіпертонічна хвороба [2].
Чинники ризику розвитку ССЗ
Метаболічні, поведінкові, екологічні та професійні
чинники ризику негативно впливають на розвиток
і прогресування ССЗ [1, 3-6]. Високий систолічний
артеріальний тиск, дієта та рівень ХС ЛПНЩ належать
до основних чинників ризику ССЗ, які становлять 25,0;
17,2 і 11,0% смертей від ССЗ відповідно [2]
Цільові рівні ХС ЛПНЩ
Більшість хворих на дисліпідемію не досягають
оптимального рівня ХС ЛПНЩ за допомогою зміни
способу життя та приймання доступних і недорогих
статинів [7-11]. Так, за даними багатоцентрового
дослідження DA VINCI, лише 33% із 5888 пацієнтів
із дисліпідемією досягали цільового рівня ХС ЛПНЩ,
рекомендованого Європейським товариством кардіо-
логів (ESC, 2019) [12]. У різних країнах Європи спо-
стерігається подібна тенденція [13-15]. Дані австра-
лійського дослід ження за участю 61 407 пацієнтів
засвідчили, що лише 36% його учасників досягли
рекомендованих рівнів ХС ЛПНЩ [16]. Проаналізу-
вавши дані 44 млн жителів США, лише 36% пацієнтів
із високим ризиком ССЗ мали рекомендований рівень
ХС ЛПНЩ <70 мг/дл (~1,8 ммоль/л) [17].
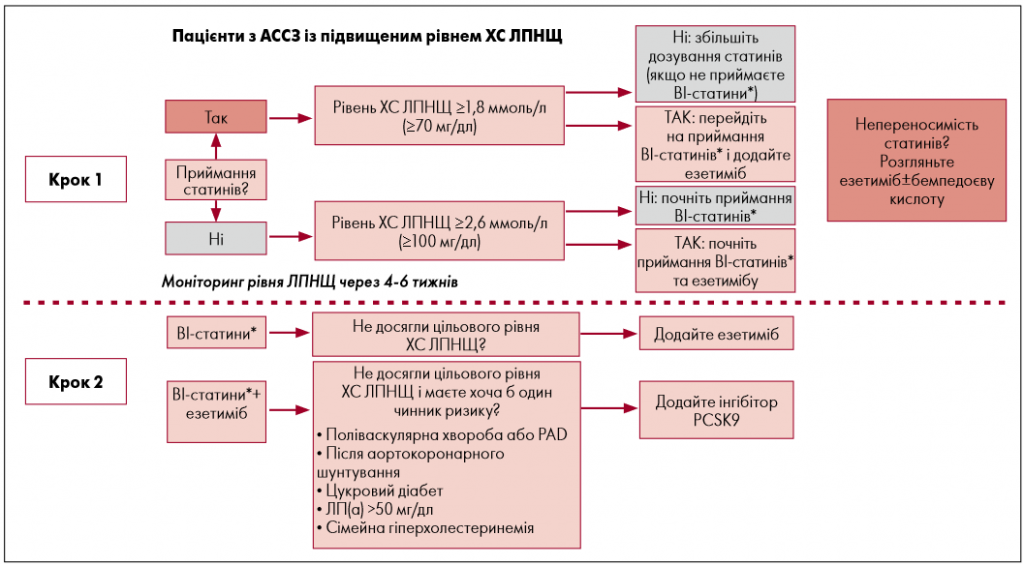
Є кілька причин, чому більшість хворих не досяга- ють необхідного рівня ХС ЛПНЩ. По-перше, згідно з рекомендаціями Європейського товариства кардіо- логів (ESC, 2019) та провідних кардіологічних спіль- нот США – Американського товариства кардіологів / Американського коледжу кардіологів (AHA/ACC, multi-society 2018) – необхідно досягати суттєвішого зниження рівня ХС ЛПНЩ, відповідно до принципу «чим нижче, тим краще» [18-20]. Наприклад, цільовий рівень ХС ЛПНЩ для пацієнтів із високим ризиком було зменшено до <1,8 ммоль/л. По- друге, просте- жується незацікавленість пацієнтів у зниженні рівня ХС ЛПНЩ завдяки зміні способу життя або регуляр- ному фармакологічному лікуванню через недостатньо швидкі результати.
Додатковою перешкодою також можуть стати високі ціни на нові препарати, як-от інгібітори PCSK9, які необхідно приймати для швидкого досягнення цілей лікування. Зважаючи на те, що 9,1% пацієнтів мають непереносимість до статинів, альтернативних підходів до зниження ХС може бути недостатньо.
Препарати для корекції дисліпідемії
У рекомендаціях ESC (2019) та AHA/ACC/multi-
society (2018) зазначено перелік фармацевтичних пре-
паратів, які можливо застосовувати для зниження рівня
ліпідів у крові та зменшення ризику ССЗ у пацієнтів
із дисліпідемією (таблиця).
Згідно із зазначеними настановами статини є першою лінією терапії для первинної та вторинної профілак- тики ССЗ у пацієнтів із гіперхолестеринемією та гіпер- тригліцеридемією.
Механізм дії статинів
Статини допомагають знизити синтез холестерину
в організмі завдяки конкурентному інгібуванню ферменту
3-гідрокси-3-метилглутарил-коензим А (ГМГ-КоА)
редуктази [19]. Зменшення синтезу холестерину в пе-
чінці зумовлює підвищення поверхневої експресії
рецепторів ХС ЛПНЩ, що, своєю чергою, збільшує
поглинання ХС ЛПНЩ, призводячи до зниження
рівня ХС ЛПНЩ, ApoB-100 і тригліцеридів у сироватці
крові. Завдяки конкурентному пригніченню ГМГ-КоА,
дозозалежну ефективність статинів використовують
у клінічній практиці для ескалації лікування від низь-
кої / середньої до високоінтенсивної терапії стати-
нами для пацієнтів групи ризику. Відомо, що статини
низької / середньої інтенсивності сприяють зниженню
рівня ХС ЛПНЩ на 30-50% і тригліцеридів на 20%, тоді
як високої інтенсивності – на >50 і 40% відповідно [19,
31]. Водночас статини можуть підвищувати рівень холе-
стерину ліпопротеїдів високої щільності (ХС ЛПВЩ)
залежно від дози застосування на 10% [32].
За даними досліджень, у пацієнтів, які отримували
статини, не виявлено значущого підвищення рівня
ліпопротеїну (a) [Lp(a)] [33, 34].
| Назва | MoA | Тип | RoA | ХС ЛПНЩ | ТГ | МАСЕ |
|---|---|---|---|---|---|---|
| Статини низької / середньої інтенсивності | Інгібування HMG-CoA- редуктази, плейотропне | Таблетки | Раз/день, п.о. | -30% | -20% | -22% |
| Статини високої інтенсивності | Інгібування HMG-CoA, плейотропне | Таблетки | Раз/день, п.о. | -50% | -40% | -15% а |
| Езетиміб | Інгібування NPC1L1 | Таблетки | Раз/день, п.о. | -24% | -12% | -6% |
| Еволокумаб | Інгібування PCSK9 | Ін’єкції | Раз на 2 тижні/ щомісяця, п.с. | -60% | -26% | -15% |
| Алірокумаб | Інгібування PCSK9 | Ін’єкції | Раз на 2 тижні/ щомісяця, п.с. | -60% | -26% | -15% |
| Фібрати | Активація PPARa | Таблетки | Раз на день, п.о. | -20% | -50% | -10% |
| Ікосапент етиловий | Зниження рівня ТГ, плейотропне | Таблетки | Двічі на день, п.о. | -6% | -20% | -25% |
| Примітка. а Наведене зниження MACE для статинів високої інтенсивності належить до додаткової переваги порівняно зі статинами низької / середньої інтенсивності. HMG-CoA – 3-гідрокси-3-метилглутарил коензим A, LDL-C – холестерин ліпопротеїнів низької щільності (ХС ЛПНЩ), MACE –основні несприятливі серцево- судинні події, MoA механізм дії, NPC1L1 – Niemann-Pick C1-like - С1 білок Німана-Піка, PCSK9 – пропротеїн конвертаза субтилізин-кексинового типу 9, PO (п.о.) – пероральний, PPAR-α – рецептор проліфератора пероксисоми альфа, RoA – шлях введення, SC – підшкірно, TG(ТГ) – тригліцериди. Адаптовано за D. T. Michaeli, 2023. | ||||||
Окрім зміни рівня ліпідів у крові, результати дослі- джень in vitro та in vivo підтвердили, що статини мають корисні кардіопротекторні плейотропні ефекти, як-от поліпшення ендотеліальної дисфункції, підвищення біодоступності оксиду азоту; антиоксидантні власти- вості, пригнічення запальних реакцій і стабілізація атеросклеротичних бляшок [35, 36]. Однак значення цих плейотропних ефектів у клінічній практиці досі лишається дискусійним [37].
Ефективність статинів Для профілактики ССЗ ефективність статинів підтвер- джується даними метааналізів [38-50]. Так, аналізуючи дані 170 тис. пацієнтів, виявлено зниження ХС ЛПНЩ на 38,67 мг/дл (1 ммоль/л), що пов’язане зі зниженням ризику серйозних серцево-судинних подій (MACE) на 22% (95% ДІ від -20 до -24; p<0,0001) на тлі терапії статинами низької / помірної інтенсивності [38].
Це підтверджує, що рівень ХС ЛПНЩ є достовір- ним сурогатним параметром для клінічних кінцевих точок MACE та серцево-судинної смерті. Подальша інтенсифікація терапії забезпечувала додаткове зни- ження ризику MACE на 15% (95% ДІ від -11 до -18; p<0,0001) [38]. Отримані результати узгоджу ються з даними в когортах осіб первинної та вторинної про- філактики [40, 41, 48, 49, 51]. У пацієнтів із низьким ризиком ССЗ (<10%) терапія статинами сприяла зни- женню ризику серйозних судинних подій (ВР 0,79; 95% ДІ 0,77-0,81 на 1,0 ммоль/л зниження ХС ЛПНЩ) незалежно від попередніх захворювань судин [40]. Завдяки статинотерапії ризик смертності від усіх при- чин знижувався на 9% на кожен 1,0 ммоль/л зниження ХС ЛПНЩ. Оскільки статини метаболізуються в пе- чінці, інгібітори та індуктори системи цитохромів P450 (CYP), зокрема протимікробні препарати, антагоністи кальцію, циклоспорин і грейпфрутовий сік, можуть призводити до міжлікарської взаємодії, що позначати- меться на їх біодоступності, а зрештою, – на збільшенні побічних ефектів або обмеженні терапевтичної дії.
Так, за даними недавнього метааналізу 176 досліджень за участю 4,1 млн пацієнтів, 9,1% осіб мали непере- носимість статинів [25]. Вік, жіноча стать, азіат ська та негроїдна (екваторіальна) раси, ожиріння, цукро- вий діабет, гіпотиреоз, хронічні захворювання печінки, ниркова недостатність, антиаритмічні препарати, бло- катори кальцієвих каналів, вживання алкоголю та ви- сокі дози статинів асоціювалися з більшим ризиком непереносимості статинів [25]. Попри те, що статини є препаратами першої лінії для корекції дисліпідемії, зокрема в осіб із гіперхолестеринемією або гіпертриглі- церидемією, у багатьох пацієнтів рівень ліпідів у крові залишається вищим за встановлені ESC (2019) цільові рівні. Упродовж останніх двох десятиліть вчені активно працювали над розробкою нових варіантів фармаколо- гічного лікування ССЗ, щоб зменшити ризик неспри- ятливих серцево-судинних подій серед пацієнтів групи ризику. Власне, сучасні засоби такої терапії рекомен- довано призначати як ад’ювант до статинів середньої / високої інтенсивності або як препарати монотерапії в пацієнтів із непереносимістю статинів.
Вплив езетимібу на дисліпідемію Езетиміб вибірково пригнічує всмоктування холе- стерину в тонкому кишечнику, не змінюючи при цьому поглинання інших поживних речовин і вітамінів [56, 57]. Молекулярною мішенню езетимібу є переносник стеролів Niemann-Pick C1-Like 1 (NPC1L1), що від- повідає за всмоктування холестерину та фітостеролів у кишечнику. Дані дослідження генетичного секвену- вання (за участю понад 90 тис. пацієнтів) підтвердили значно нижчі рівні ХС ЛПНЩ і менший ризик ішеміч- ної хвороби серця в пацієнтів із мутаціями NPC1L1 [58].
За даними досліджень, порівняно з монотерапією ста- тинами, їх комбінація з езетимібом знижувала рівень ХС ЛПНЩ на 24%, ApoB-100 – на 14%, тригліцери- дів – на 12% і високочутливого С-реактивного білка (hsCRP) – на 13% [59-61]. Відповідно до результатів рандомізованого контрольованого подвійного сліпого дослідження IMPROVE-IT, яке налічувало 18 144 паці- єнтів після гострого коронарного синдрому з подаль- шим спостереженням упродовж 6 років, езетиміб, який додавали до симвастатину, порівняно з монотерапією симвастатином, знижував ризик MACE на 6% (95% ДІ від 1 до 11; p=0,016).
Дані дослідження ENHANCE не підтвердили, щодода- вання езетимібу до статинів значно зменшує товщину інтими та медіа в пацієнтів із сімейною гіперхолестерине- мією, хоча результати дослідження SHARP і SEAS засвід- чили ефективність езетимібу для профілактики ішемічних серцево-судинних подій [62-65]. Безпеку та ефективність застосування езетимібу також було підтверджено числен- ними даними метааналізів [61, 66-70].
Зокрема, у дослід жен ні EWTOPIA-75 вивчали ефективність монотерапії езетимібу для первинної серцево-судинної профілактики в пацієнтів віком >75 років. Для приймання езетимібу (10 мг на день) 3796 пацієнтів розподілили у випадковий спосіб, щоб порівняти отриманий ефект зі звичайним лікуванням. Після середнього періоду спостереження 4,1 року застосування езетимібу знизило частоту MACE на 34% (ВР 0,66; 95% ДІ 0,50-0,86; p=0,002) [71]. Порівняно з монотерапією статинами, ад’ювантна терапія езети- мібом не збільшувала частоту виникнення побічних ефектів і не призводила до припинення лікування.
Висновки
Для запобігання серцево-судинним подіям нині між-
народні наукові групи активно працюють над розроб-
кою нових препаратів, що допомагатимуть ефективно
знижувати рівень ліпопротеїнів. Комбіновану терапію
широко застосовують для лікування артеріальної гіпер-
тензії, а віднедавна – і дисліпідемії. Основною метою
розробки поєднання комбінацій препаратів є підвищен-
ня ефективності терапії завдяки мінімізації частоти не-
бажаних побічних ефектів і поліпшення прихильності
пацієнта до лікування. На думку S.R. Gnanenthiran et al.
(2023), комбінована терапія препаратами з фіксованими
дозами діючих речовин в одній таблетці (single-pill)
може сприяти доповненню та поліпшенню наявних
стратегій для зменшення загального ризику ССЗ.
Сьогодні на фармринку України комбінований засіб розувастатину та езетимібу представлено препаратом Розуліп® Плюс (виробник ЗАТ «Фармацевтичний завод «ЕГІС»). Рекомендована добова доза препарату – одна капсула (містить 10 мг розувастатину і 10 мг езетимібу або 20 мг розувастатину і 10 мг езетимібу), яку прийма- ють незалежно від вживання їжі. Розуліп® Плюс є пре- паратом вибору для комбінованої ліпідознижувальної терапії. Терапевтичний ефект спостерігається впродовж 1-го тижня після початку лікування, через 2 тижні він досягає 90% можливого, а через 4 тижні – максималь- ного рівня.